



数辉自研的深度生成式AI模型的蛋白质动态结构预测模型(DeepConformer)基于深度生成式AI算法,能够从蛋白质序列出发直接预测出蛋白质三维结构的动态构象。我们的动态构象预测算法可以快捷地获取蛋白质分子的动态特征,并直接应用于基于蛋白质构效关系的蛋白质设计流程,以及蛋白质理化性质预测优化等多种任务场景。

数辉自研的蛋白生成平台充分利用深度生成模型的强大建模能力,深入研究蛋白质序列的进化规律和隐含关系,以期为药物设计、酶工程等领域提供全方位的解决方案。通过生成具备多样性和自然物理特性的序列变体,平台为未来药物研发、生物工程等领域的创新和发展奠定了坚实基础。

数辉综合使用多种分子动力学模拟方法,获取蛋白质分子的动态特征,探索蛋白质分子的活性位点和功能机制。通过构建构象与功能机制之间的联系,助力生物分子的设计和优化。蛋白质分子模拟在提供以及辅助生成蛋白质构象、蛋白质与其他分子的活性位点和相互作用机制研究、蛋白质稳定性预测和蛋白质亲和力计算等多种应用场景中均能发挥作用。

抗体的 Fab 区域(片段抗原结合区)是抗体上与抗原结合的区域。由重链和轻链各一个 恒定结构域和一个可变结构域组成,执行一系列对免疫反应至关重要的功能。数辉基于 公开数据库抗体 Fab 序列及结构数据,开发了对抗体 Fab 区域的端到端结构预测模型, 能够基于序列信息对恒定区及可变区(CDR Loops)进行高精度的预测。模型可帮助研 究人员全面了解抗体的总体结构和功能,提供抗体-抗原相互作用机制的见解,可应用于 治疗性抗体的设计、疫苗开发以及抗体性质改造等场景。

RNA作为精确调控基因表达和蛋白质合成的工具,对于疾病治疗和生物工程非常有价值。数辉的RNA设计平台利用尖端的深度生成模型的高效算法,深入解析RNA序列、结构与功能,从而可以精准设计RNA分子,助力创新的医药研发和生物技术突破。平台的序列生成方法能够高比例生成具有活性的IRES序列,可用于简化基因治疗载体的设计,以及在合成生物学中构建精密的基因电路等多种应用。

涵盖了基于AI模型的适配体二级结构预测平台、核酸-蛋白复合物三级结构预测平台、适配体-蛋白相互作用预测平台以及分子模拟探索/验证核酸-蛋白结合机制等功能。其中,适配体-蛋白相互作用预测平台利用自然语言模型捕捉蛋白序列和适配体序列的高级特征以预测适配体与蛋白质结合的可能性。该平台利用了数辉自建的适配体相互作用数据库训练,得到的适配体序列经分子模拟验证对突变敏感度高。适配体-蛋白相互作用预测平台旨在为快速筛选可与靶标蛋白结合的适配体序列。

蛋白质功能改造是通过改变其氨基酸序列或结构来提升其特定功能的过程。数辉以蛋白质的预训练语言模型为基础,利用深度学习技术和内外部数据集,结合了蛋白质的大规模表征和图网络表示方法进行功能预测模型开发。改造同事结合动态构象模型及分子模拟分析,对催化活性,热稳定性,亲和力等蛋白功能进行预测,提升或改造,专注于对突变和特异度敏感的功能预测模型。
这包括提高酶的催化效率、增强蛋白质的热稳定性、增加与目标分子的亲和力及特异性等。以蛋白质的预训练语言模型为基础,数辉设计出对序列突变具有高特异性和灵敏度的蛋白质性质预测模型,协助开发更有效的生物催化剂和工业酶等。
蛋白质成药性相关属性包括但不限于溶解度、聚集、半衰期、稳定性、毒性、免疫原性等。通过多模态融合架构的深度学习网络,数辉能够有效预测这些成药性相关属性,显著提升了成药性各属性的预测的准确性和鲁棒性。

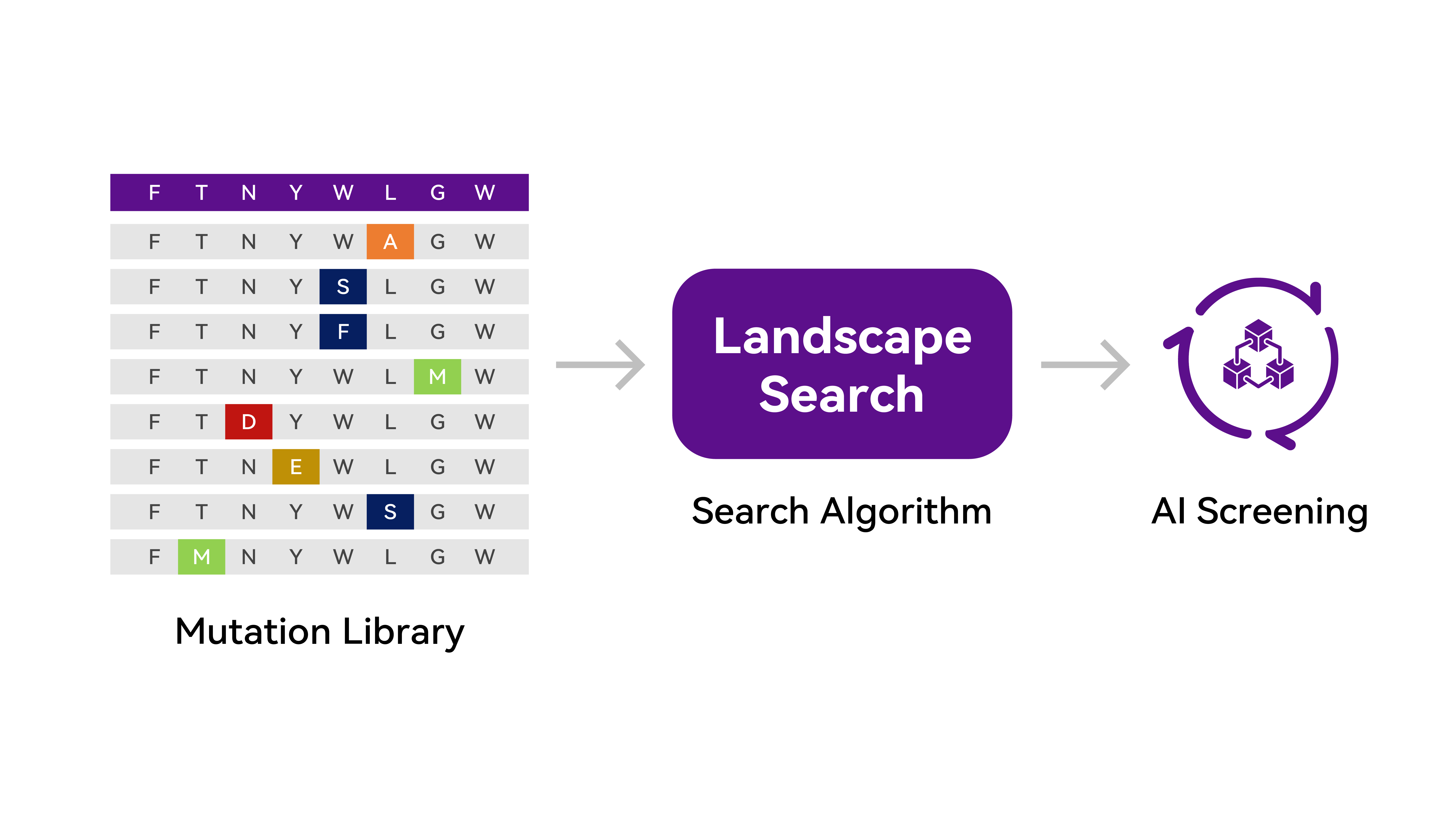
针对特定的预测目标与不同的业务场景,组合数辉特色的分子模拟技术与动态构象预测能力。从生成到预测再到改进,实现高通量覆盖。基于数辉先进的多目标优化算法,在单点、多点甚至是全位点上探索蛋白质拓扑结构的复杂性,实现蛋白功能优化、酶活性改造的核心指标提升。
序列进化与溯源是揭示生命起源、理解生物多样性和开发新型治疗方法的关键研究方法。通过分析生物分子的序列信息,数辉可以追踪基因和蛋白质的演变过程,识别关键的进化事件,并预测未来的进化趋势。生物序列的进化是通过突变、重组和选择等机制推动的。这些机制在分子水平上产生了丰富的遗传多样性。通过比较不同生物体的基因或蛋白质序列,揭示它们之间的进化关系。序列溯源在疾病研究、疫苗开发和生物技术等领域具有广泛应用。
